Ja, helaas loopt je huisdier ook het risico om COVID-19 te krijgen. Net zoals wij vatbaar zijn voor infectie met het SARS-CoV-2 virus, zijn bepaalde diersoorten dat ook. Omdat dieren vergelijkbare structurele kenmerken hebben van de eiwitten aan het celoppervlak die aanwezig zijn bij mensen.
Een specifiek aanwezig eiwit werkt als een slot- en sleutelsysteem, waarbij de sleutel het viruseiwit is dat verantwoordelijk is voor COVID-19-infectie en het slot het membraaneiwit is dat zich op het celoppervlak bevindt.
Als de sleutel - het viruseiwit - op het slot past - het receptoreiwit van de gastheer - dan kan het virus naar binnen en zijn vermenigvuldigingscyclus starten, waardoor de gastheer geïnfecteerd raakt.
Een onderzoek gepubliceerd op PLOS Computational Biologygebruikte een wiskundig model om te voorspellen welke diersoorten de noodzakelijke kenmerken van het gastheereiwit hebben waardoor het virus het spikeiwit kan binden.
Onderzoekers meldden enkele gevallen over de hele wereld van huisdieren, boerderijdieren en dieren in dierentuinen die positief testten op een COVID-19 infectie.
Katten, nertsen, leeuwen en tijgers zijn enkele soorten die als besmet zijn gemeld.
Aanvankelijk toonden studies aan dat katten, civetkatten en fretten gevoelig waren voor SARS-CoV-2, terwijl varkens, kippen en eenden dat niet waren.
Op een tweede moment kwamen er andere resultaten naar voren, waarbij cavia's, muizen en ratten als niet vatbaar werden geclassificeerd, terwijl kamelen, runderen, paarden, schapen en konijnen als vatbaar voor SARS-CoV-2 infectie werden geclassificeerd.
We moeten niet vergeten dat het SARS-CoV-2 virus voor het eerst werd overgedragen op mensen via een tussengastheer.
De twee belangrijkste verdachte dieren zijn vleermuizen en schubdieren. Als het de eerste keer is dat je van schubdieren hoort, het zijn nachtdieren bedekt met keratine schubben die leven in holle bomen en holen.
Hier is een illustratie van een schubdier:
Om de infectie te starten, moet het virus eerst zijn virale spike-eiwit binden aan het receptoreiwit van het membraan van de gastheercel.
Het gastheerreceptoreiwit is een extracellulair proteasedomein van angiotensine-converterend enzym 2, meestal bekend als ACE2.
ACE2 is een single-pass transmembraan eiwit dat aanwezig is op het oppervlak van verschillende weefsels. ACE2 heeft niet slechts één structuur, het kan meerdere structuren hebben bij verschillende soorten met behoud van dezelfde functie.
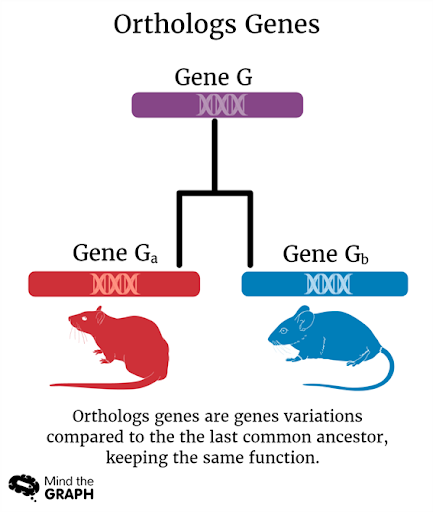
In feite is ACE2 geclassificeerd als een ortholoog gen, dat wil zeggen, een gen dat aanwezig is in verschillende soorten dat afstamt van een gemeenschappelijk voorouderlijk gen.
Deze structurele verschillen zijn blijkbaar de reden waarom het virus SARS-CoV-2 kan binden aan de ACE2 van sommige soorten en niet aan die van andere.
Zodra het virale spike-eiwit is verbonden met de ACE2, dringt het virus de cel binnen en begint het de celmechanismen van de gastheer te gebruiken om zich te vermenigvuldigen, wat leidt tot infectie.
Als gevolg hiervan zou een beter begrip van de ACE2 receptor zeker leiden tot een preciezere verklaring waarom sommige diersoorten gevoelig zijn voor infecties en andere niet.
Daarnaast zou het wetenschappers ook helpen bij de ontwikkeling van medicijnen, door antivirale strategieën toe te passen, zoals het produceren van nepkastjes waaraan het virus zich kan binden in plaats van het echte kastje van de gastheer.
Maar ook om gastheren beter op te sporen voor toekomstige virusinfecties.
Dus, het karakteriseren van de driedimensionale structuur van ACE2 en zijn interacties op atomair niveau met behulp van computermodellen was het doel van Rodrigues en collega's werken.
Dit type karakteriserend onderzoek is experimenteel duur en niet toepasbaar op grote schaal, waardoor het moeilijk is om sluitende gegevens te verkrijgen, terwijl computermodellering snel en goedkoop is en zeer nuttig is om enkele hiaten in de kennis van het structurele raamwerk op te vullen.
In het onderzoek werden 28 diersoorten geanalyseerd en werd een 3D-model gegenereerd van het ACE2-eiwit dat aan het virale spike-eiwit is gebonden.
De resultaten toonden aan dat er sleutellocaties zijn in de ACE2-aminozuursequentie, waar het virale eiwit door mutaties niet kon binden aan de gastheercel.
In de ACE2-sequentie ontbreekt één aminozuur dat verantwoordelijk is voor een intermoleculaire zoutbrug tussen ACE2 en de bindingsplaats van het virale eiwit, zoals gerapporteerd door Rodrigues en zijn team.
Dit resultaat wordt ondersteund door andere gepubliceerde onderzoeken, die experimenteel hebben aangetoond dat het deze mutant ontbreekt aan een negatief geladen aminozuur, waardoor het virale eiwit zich kan binden.
Het onderzoek geeft ook aan dat de SARS-CoV-2 infectie complexer is dan eerder gedacht, met meer dan één manier om de gastheer te infecteren.
Het is dus belangrijk om te verduidelijken dat het verminderen van de ACE2-beschikbaarheid de kans op infectie kan verkleinen; dit voorkomt echter niet dat de infectie optreedt.
En dat de rekenmodellen niet alleen kunnen worden gebruikt om het risico op infectie bij soorten te voorspellen - er zijn aanvullende experimentele gegevens nodig om tot een betrouwbaardere conclusie te komen.
Dus ik denk dat we de pandemieprotocollen moeten blijven volgen en moeten doen wat we al doen... Maskers gebruiken, zoveel mogelijk sociale afstand houden, niet naar binnen gaan en drukke ruimtes, voor onze veiligheid en vooral voor onze geliefde huisdieren, onszelf en onze familie.
Deze pluizige kat is zo mooi, nietwaar? Je kunt deze en vele andere dierenillustraties vinden in Mind the Graph platform.
Diergeneeskunde, ornithologie, entomologieen zoölogie Op het platform zijn ook illustraties beschikbaar die je kunt gebruiken in je infographic. Mind the Graph gebruiken op dit moment!

Abonneer u op onze nieuwsbrief
Exclusieve inhoud van hoge kwaliteit over effectieve visuele
communicatie in de wetenschap.